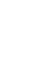Раствор – это однородная (гомогенная смесь), состоящая из растворителя и растворённого вещества
Растворитель – это вещество, которого больше в растворе и он имеет такое же агрегатное состояние, как и раствор
Растворенное вещество – это вещество, которого меньше в растворе, он может иметь любое агрегатное состояние
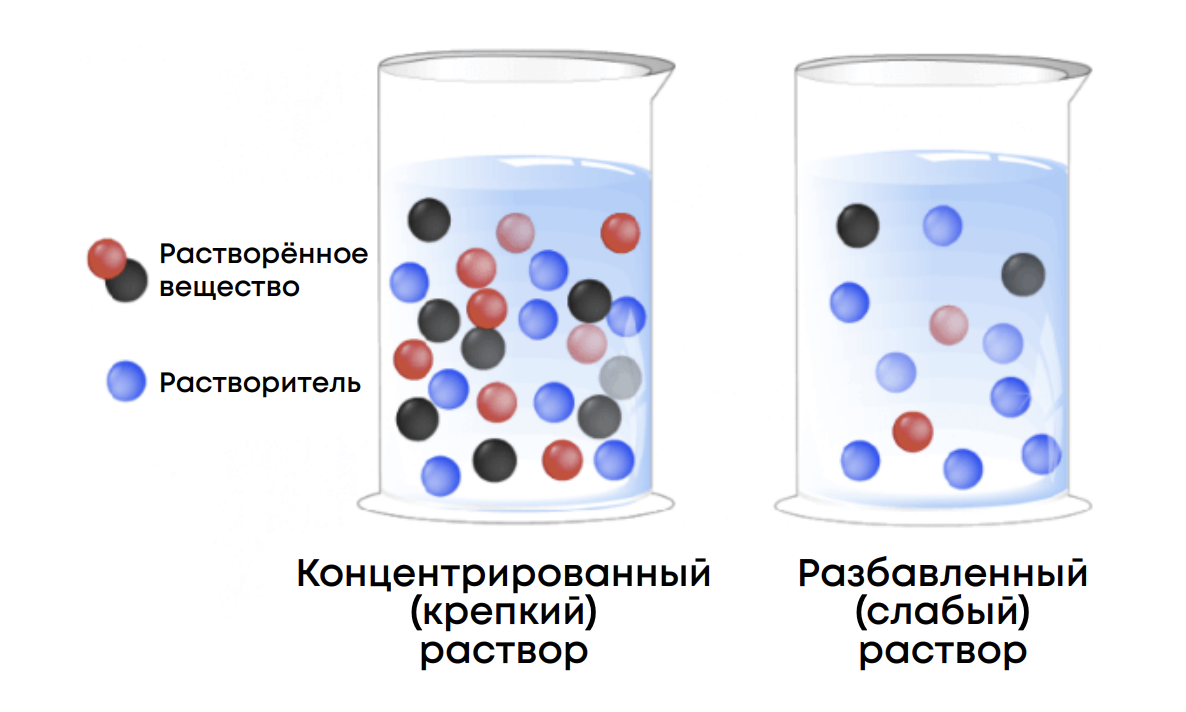
Виды растворов:
Важно: в школе под растворами чаще всего подразумевают жидкие растворы, где растворителем является вода, но растворы могут иметь любое агрегатное состояние и растворитель тоже может быть разным
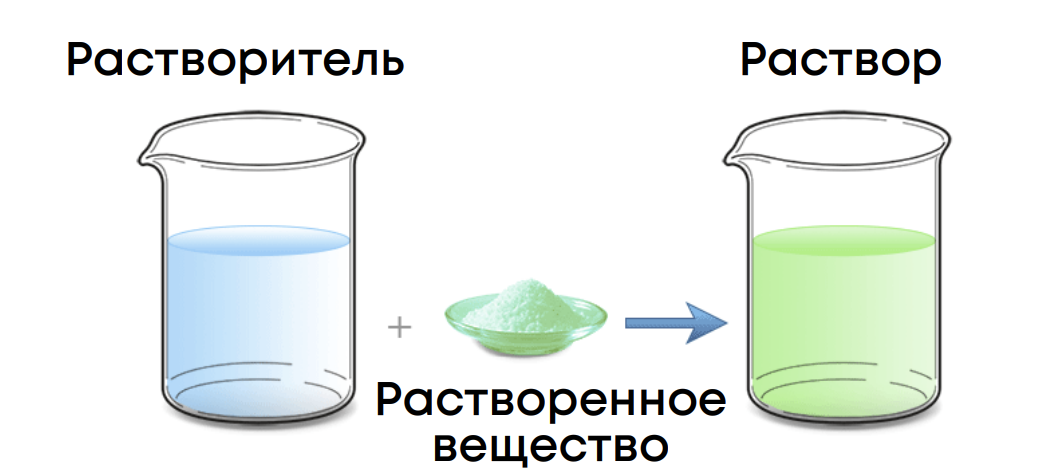
Концентрация раствора – величина, количественно характеризующая количество вещества в растворе или смеси
Массовая доля растворённого вещества (процентная концентрация) – способ выражения концентрации в процентах или в долях, отношение массы растворённого вещества к массе раствора (не растворителя!)
Формулы массовой доли растворённого вещества:
Масса раствора – сумма масс растворителя и растворённого вещества:
![]()
Массовая доля в десятичных долях:
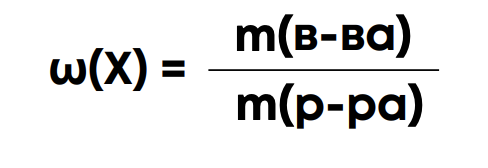
Массовая доля в процентах:

m(р-ра) – масса раствора, г
m(в-ва) – масса растворенного вещества, г
ω(X) – массовая доля растворенного
вещества X в долях (0,01) или процентах (1%)
Есть и другие способы выражения концентрации раствора (в ОГЭ нет):
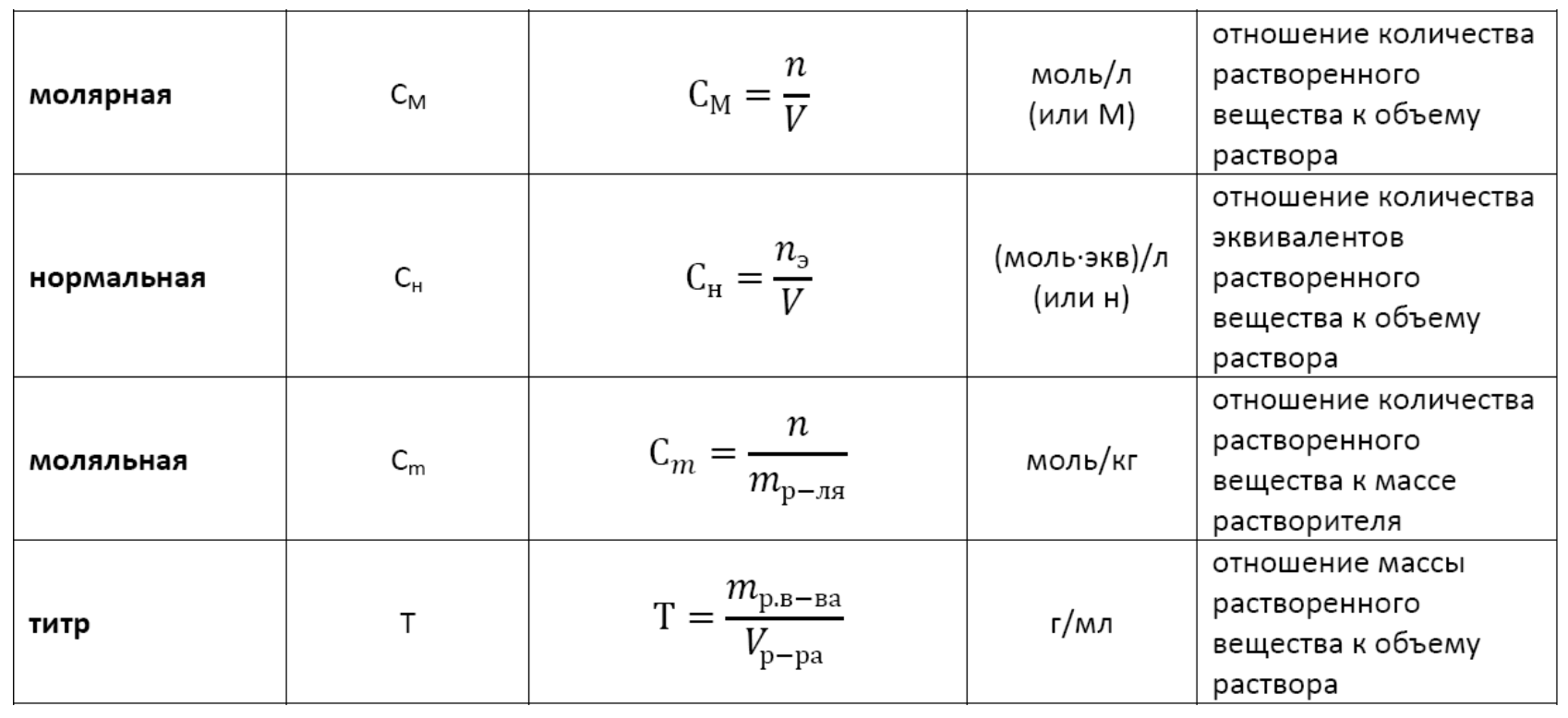
Растворимость – характеристика насыщенного раствора, которая говорит о способности вещества растворятся в растворителе (обычно воде) при данной температуре
Виды растворов по растворимости:
1 – ненасыщенный раствор: вещество ещё можно растворить
2 – насыщенный раствор: вещество больше растворить не получится
3 – пересыщенный раствор: вещество выпадает в осадок

Задача 1. В 750 г воды растворили 200 г соли. Чему равна массовая доля растворённой соли в процентах (с точностью до десятых)?
1) Найдём массу раствора:
m(р-ра) = m(ве-ва) + m (раст-ля) = 200 + 750 = 950 г
2) Вычислим массовую долю по формуле:
ω = m(ве-ва) : m(р-ра)∙100% = 200 : 950∙100% = 21,0525%
3) Округлим ответ до десятых:
21,0525% ≈ 21,1%
Задача 2. Приготовили 500 г раствора кислоты 25%. Чему равна масса кислоты в растворе (с точностью до целых)?
1) Немного перестроим формулу массовой доли и выразим массу растворённого вещества:
m(в-ва) = m(р-ра)∙ω : 100%
2) Подставим условия в формулу:
m(в-ва) = 500∙25% : 100% = 125 г
Задача 3. Приготовили раствор щёлочи, растворив 37 г щёлочи в воде и получили раствор с концентрацией 23%. Чему равна масса раствора (с точностью до целых)?
1) Немного перестроим формулу массовой доли и выразим массу раствора:
m(р-ра) = m(ве-ва) : ω∙100%
2) Подставим значения из условий в формулу:
m(р-ра) = 37 : 23%∙100% = 160,8696 г
3) Округлим ответ до целых:
160,8696 г ≈ 161 г