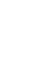Ещё из курса природоведения или окружающего мира мы знаем, что вещество может иметь разные агрегатные состояния: жидкое, твёрдое и газообразное. Агрегатные состояния у веществ зависят от внешних условий и могут изменяться.
На самом деле агрегатных состояний веществ гораздо больше, но нас интересуют эти три основные, т.к. остальные существуют в достаточно экзотических условиях (очень высокая или низкая температура, сверхвысокое давление и т.д.).
Агрегатное состояние – физическое состояние вещества, которое зависит от температуры и давления; принято выделять три основных агрегатных состояния: газ, твёрдое тело и жидкость
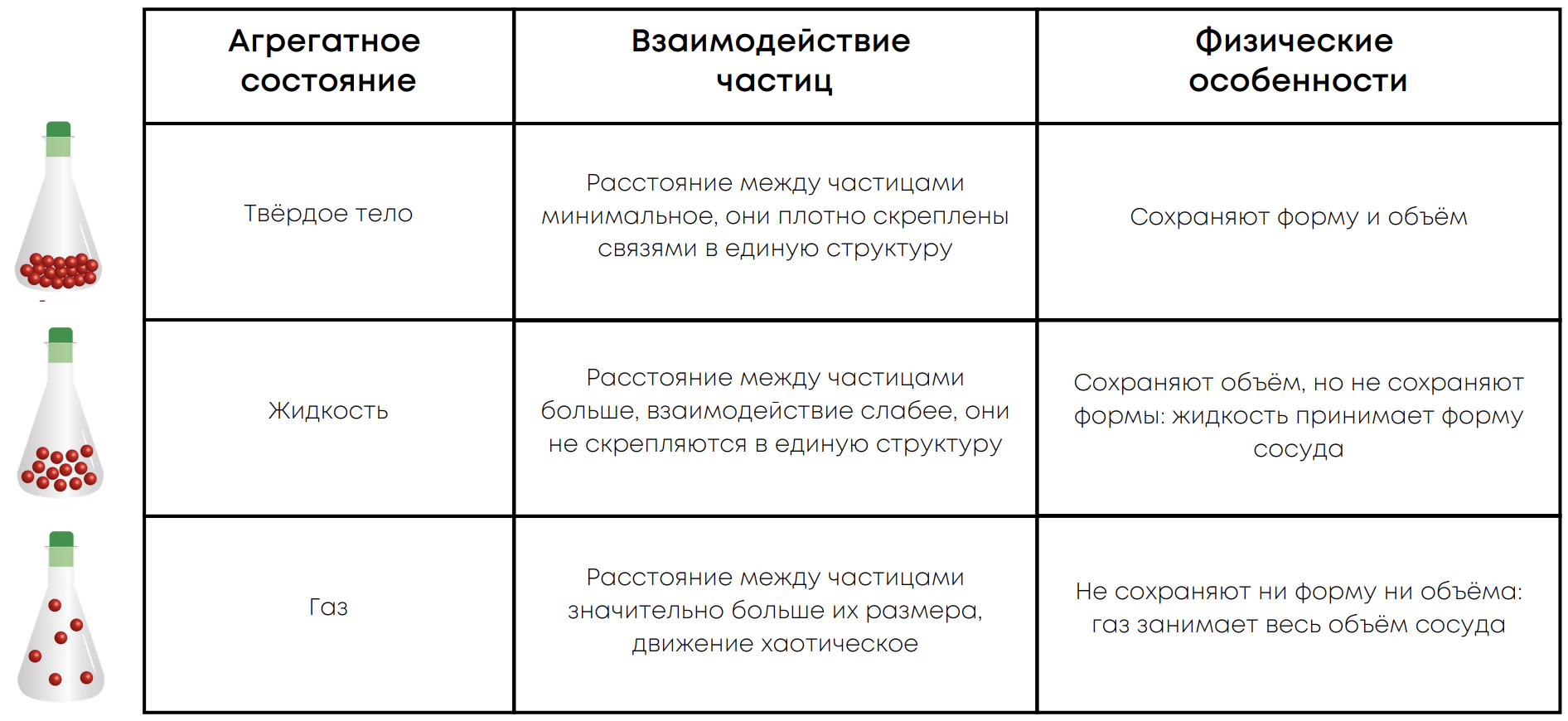
Фазовый переход – изменение агрегатного состояния вещества при изменении температуры и давления
Названия фазовых переходов:

Вещества в твёрдом состоянии различаются по расположению частиц в пространстве на кристаллическое строение и аморфное строение.
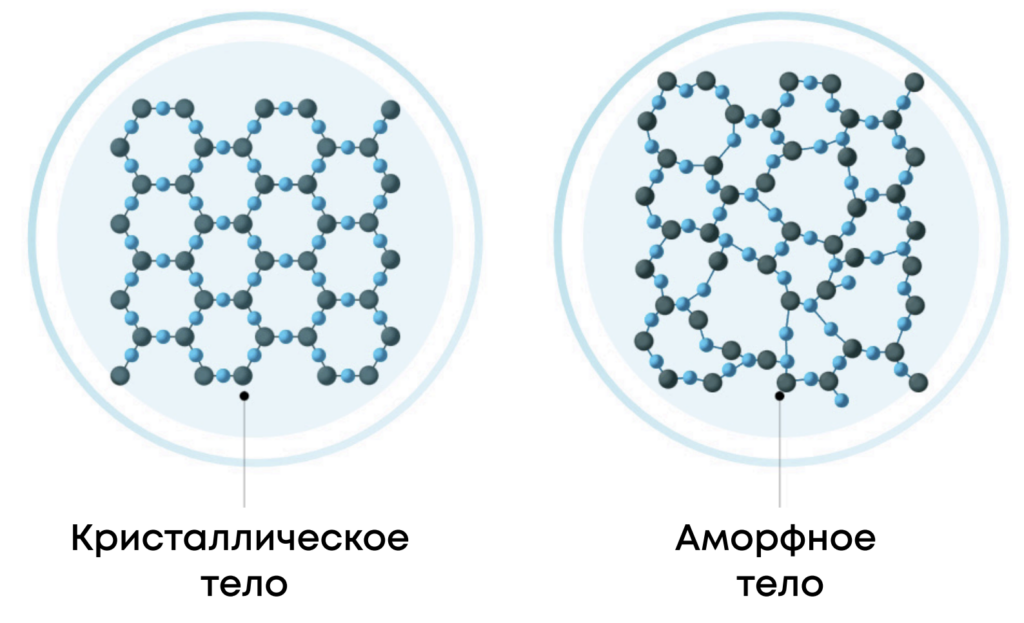
Аморфное строение – строение веществ в твёрдом состоянии, когда они расположены без четкой структуры
Особенности: изотропны, плавятся в широком диапазоне, застывают без граней, постепенно размягчаются
Примеры: стёкла, смолы, пластики, янтарь, воски, клеи
Кристаллическое строение – строение веществ в твёрдом состоянии, когда они расположены с образованием чёткой кристаллической структуры
Особенности: имеют точку плавления, застывают с гранями, разламываются на кристаллы определённой формы, анизотропны
Примеры: металлы, углекислый газ, алмаз, соли
Для справки:
Изотропия – явление, когда в веществе свойства не зависят от направления
Анизотропия – явление, когда в веществе свойства зависят от направления (например дрова легко раскалываются вдоль волокон, но тяжело поперёк)
Ранее мы с вами говорили о том, что вещества состоят из молекул. Это правда, но только отчасти: существуют вещества молекулярного и немолекулярного строения. В немолекулярном строении можно выделить три типа: ионное, атомное и металлическое.
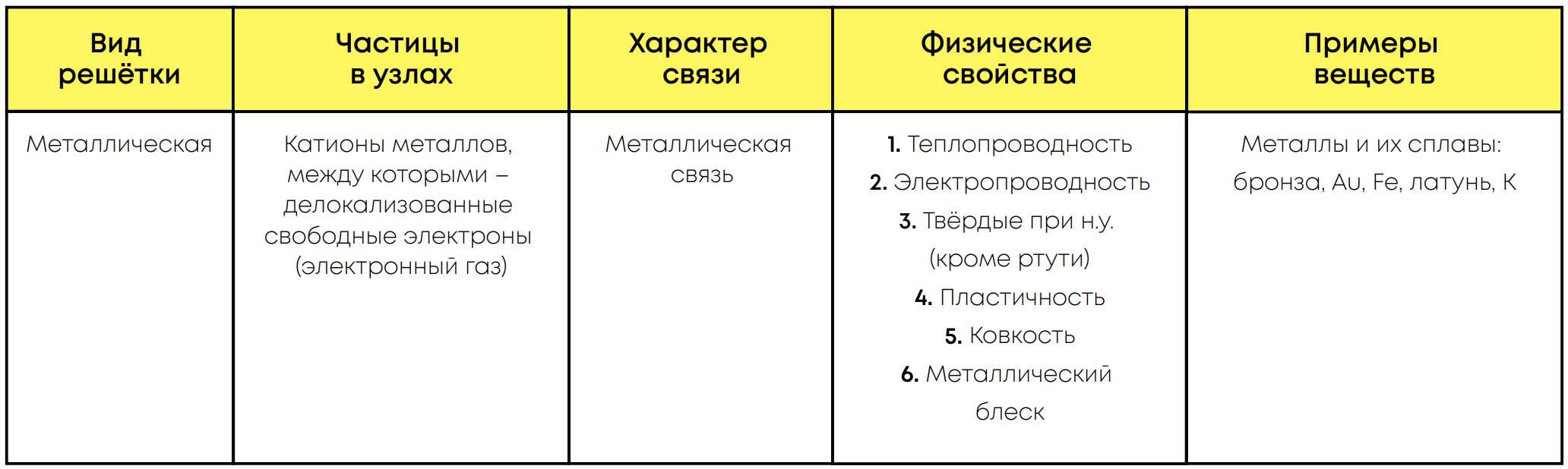
Кристаллическая решётка – геометрический образ, показывающий порядок расположения частиц в узлах (место расположения частиц) твёрдой кристаллической структуры
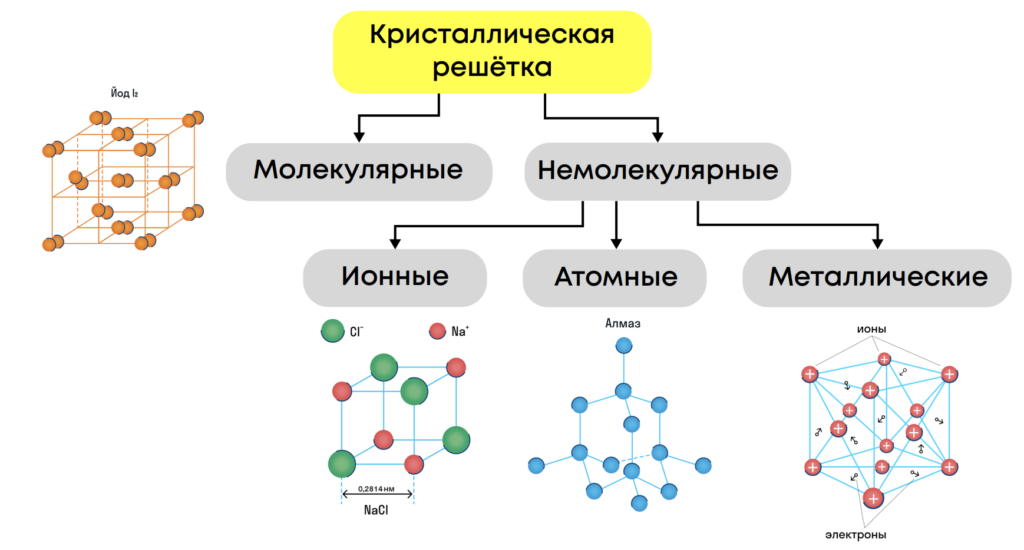
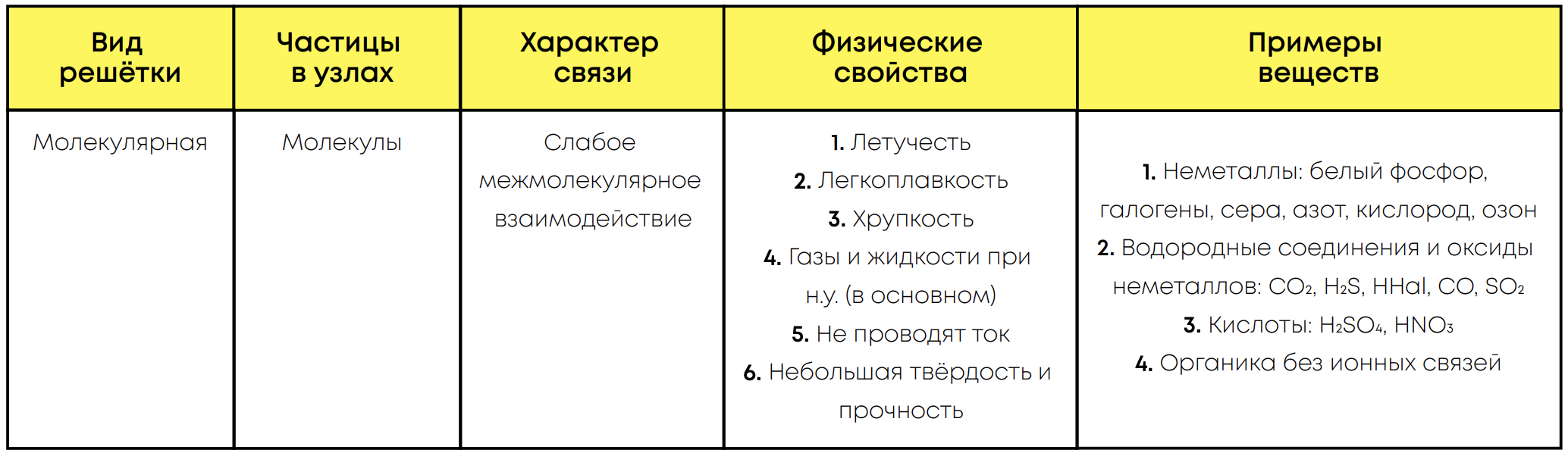
Молекулярная решётка образуется из молекул, связанными слабыми межмолекулярными взаимодействиями.
Ионная решётка образуется из ионов, связанных ионными связями.

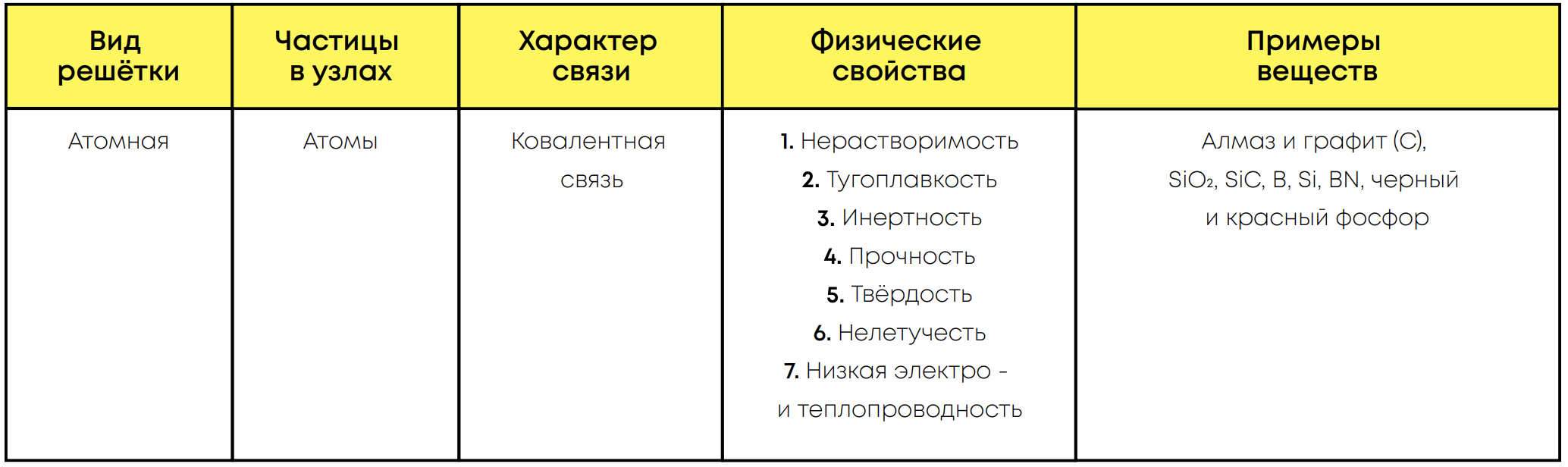
Атомная решётка образована атомами, связанными ковалентными связями.
Металлическая решётка образована катионами металлов и свободными электронами между ними, связанными металлическими связями.