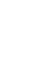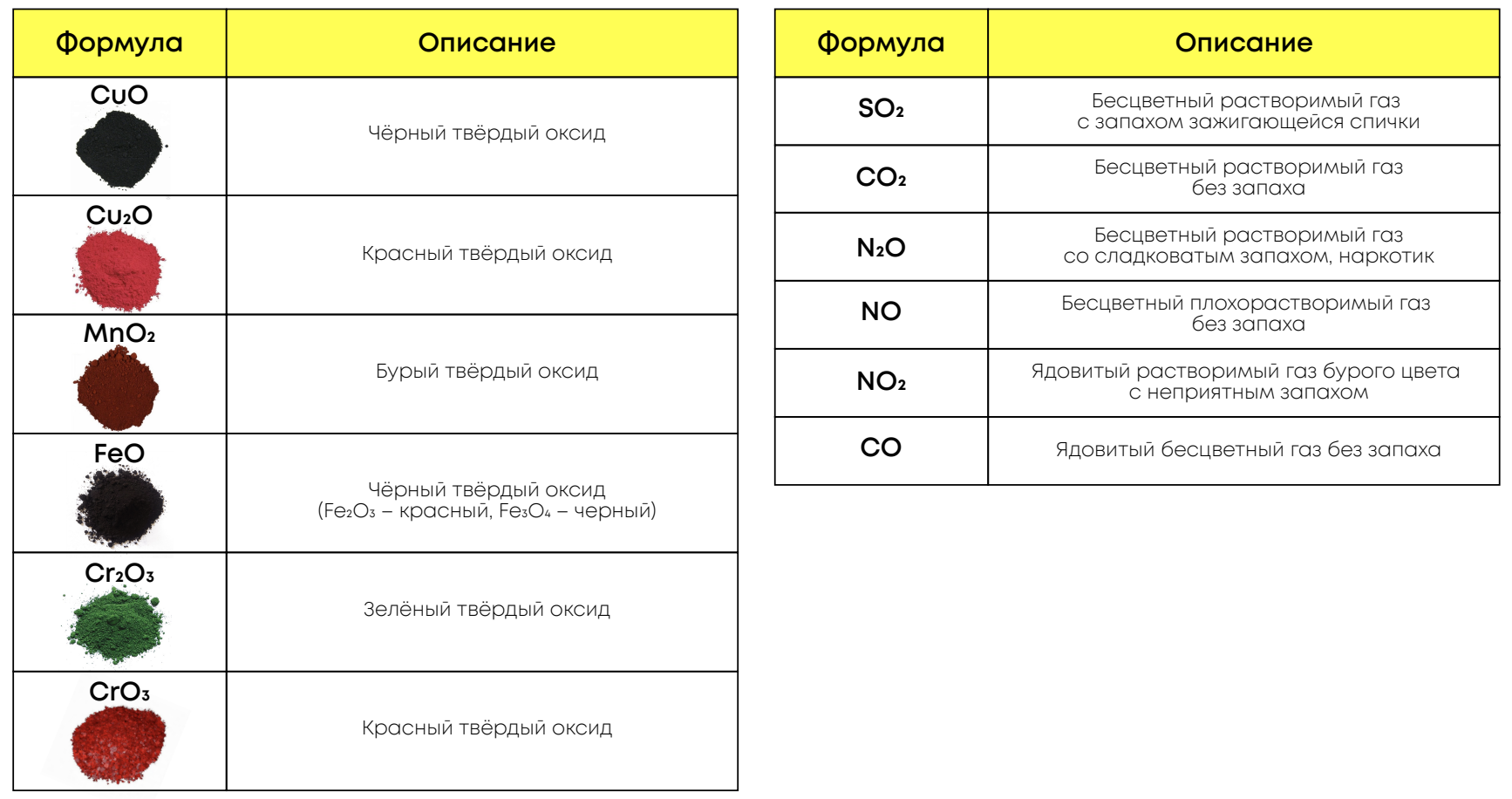
Химические свойства основных оксидов:
Основные оксиды щелочных и щелочноземельных металлов мы для краткости называем активными основными оксидами.
1. С водой (если в реакции образуется щёлочь):
BaO + H2O → Ba(OH)2
Исключение при кипячении:
MgO + H2O → Mg(OH)2↓
2. С кислотными оксидами:
Na2O + SO3 → Na2SO4
3. С амфотерными оксидами (только активные оксиды):
Na2O + Al2O3 → 2NaAlO2
4. С кислотами:
CuO + 2HNO3 → Cu(NO3)2 + H2O
5. С амфотерными гидроксидами (только активные оксиды):
Na2O + 2Al(OH)3 → 2NaAlO2 + 3H2O
Химические свойства амфотерных оксидов:
1. С водой – не реагируют!
2. С основными оксидами (только с активными оксидами):
Na2O + BeO → Na2BeO2
3. С кислотами:
Al2O3 + 6HCl → 2AlCl3 + 3H2O
4. С щелочами:
Al2O3 + 2NaOH → 2NaAlO2 + H2O – при сплавлении до алюмината
Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4] – при растворении до тетрагидроксоалюмината
ZnO + 2NaOH → Na2ZnO2 + H2O – при сплавлении для цинката
ZnO + 2NaOH + H2O → Na2[Zn(OH)4] – при растворении до тетрагидроксоцинката
5. С солями (вытеснение более летучего оксида):
Na2CO3 + Al2O3 → 2NaAlO2 + CO2↑
Na2SO3 + ZnO → Na2ZnO2 + SO2↑
Химические свойства кислотных оксидов:
1. С водой (кроме SiO2):
SO3 + H2O → H2SO4
2. С основными оксидами:
CaO + SO2 → CaSO3
3. С амфотерными оксидами:
ZnO + SO3 → ZnSO4
4. С основаниями:
KOH + SO3 → KHSO4 – избыток кислотного оксида
2KOH + SO3 → K2SO4 + H2O – избыток щёлочи
5. С амфотерными гидроксидами:
SO3 + Zn(OH)2 → ZnSO4 + H2O
6. С солями более слабых кислот:
CO2 + H2O + Na2SiO3 → Na2CO3 + H2SiO3↓ – в растворе
SiO2 + K2CO3 → K2SiO3 + CO2↑ – сплавление
SiO2 + Na2SO3 → Na2SiO3 + SO2↑ – сплавление
Запоминалка:
Давным-давно на земле рулили жизнью три клана: люди, волки и оборотни. Волки постоянно воевали против людей, а люди – против волков. Оборотни, которые были наполовину людьми и наполовину волками, бились и с людьми и с волками. Многие считали их двуличными. Но никто не воевал против своего клана!

Специфические свойства:
1. Взаимодействие с кислородом (только невысшие оксиды):
4FeO + O2 → 2Fe2O3
4Fe3O4 + O2 → 6Fe2O3
2Cu2O + O2 → 4CuO
2SO2 + O2 ⇄ 2SO3 – катализатор V2O5
2. Восстановление при нагревании (Me, C, CO, NH3):
CuO + H2 → Cu + H2O
Fe2O3 + 2Al → Al2O3 + 2Fe – алюмотермия (алюминотермия)
FeO + CO → Fe + CO2
FeO + C → Fe + CO
CuO + Cu → Cu2O
3CuO + 2NH3 → N2 + 3Cu + 3H2O
Fe2O3 + Fe → 3FeO
SiO2 + C → Si/SiC + CO – зависит от избытка
SiO2 + Mg → Si/Mg2Si + MgO – зависит от избытка
SiO2 + Si → 2SiO
CO + 2H2 ⇄ CH3OH – на катализаторах и при давлении образуется метанол
2N2O + S → 2N2 + SO2
2NO + 2Mg → N2 + 2MgO
2NO + 2H2 → N2 + 2H2O
3. Другие специфические свойства:
2HgO → 2Hg + O2↑
2Ag2O → 4Ag + O2↑
SiO2 + 4HF → SiF4 + 2H2O – плавиковая кислота растворяет стекло
2NO2 + H2O → HNO3 + HNO2
2NO2 + 2KOH → KNO2 + KNO3 + H2O
4NO2 + O2 + 2H2O → 4HNO3
4NO2 + O2 + 4KOH → 4KNO3 + 2H2O
CO + Cl2 → COCl2 – ядовитый фосген (химическое оружие)
CO + NaOH → HCOONa – образуется соль муравьиной кислоты – формиат